全基因组亚硫酸氢盐测序原理
表观遗传学研究证实,特定基因区域的DNA甲基化修饰在染色体构象和基因表达调控中起着重要作用。C5(5)处DNA胞嘧啶残基的甲基化我C) 是许多真核生物中常见的表观遗传标记,广泛存在于CpG或CpHpG(H=a,T,C)中。主要有三种方法,包括内切酶消化、亲和富集和亚硫酸氢盐转化(表1)。几乎所有的序列特异性DNA甲基化分析方法都需要在扩增或杂交之前进行甲基化依赖性处理,以保持保真度。随后进行各种分子生物学技术,如下一代测序(NGS),以检测5我C残留物。
表1。基于NGS的甲基化分析的主要原理。
|
|
酶消化 |
亲和富集 |
亚硫酸氢钠 |
|
原则 |
一些限制性内切酶,如 百帕II和 Sma公司I、 被抑制5我C在CpG中。 | 亲和富集使用针对5的特异性抗体我C或甲基结合蛋白,具有DNA甲基化分析的亲和力。 | 亚硫酸氢钠通过化学方法将未甲基化的胞嘧啶转化为尿嘧啶,从而实现了甲基化检测。 |
|
方法示例 |
甲基序列
*MCA序列 *帮助序列 *MSCC |
*MeDIP序列
*MIRA序列 |
*RRBS
*WGBS *BSPP |
*MCA:甲基化CpG岛扩增;*帮助: 百帕II通过连接介导的PCR富集微小片段;*MSCC:甲基化敏感切割计数;*MeDIP-seq:甲基化DNA免疫沉淀;*MIRA:甲基化CpG岛回收试验;RRBS:亚硫酸氢盐测序的代表性降低;*WGBS:全基因组亚硫酸氢盐测序;*BSPP:亚硫酸氢盐挂锁探头。
亚硫酸氢盐的转化在20世纪90年代引发了基因组甲基化分析的革命。由于亚硫酸氢盐可以将基因组中的非甲基化胞嘧啶转化为尿嘧啶,然后在PCR扩增过程中被胸腺嘧啶取代,因此可以通过测序后对每个位置的胞嘧啶和胸腺嘧啶进行计数来与最初被甲基化修饰的胞嘧啶区分开来(图1)。 全基因组亚硫酸氢盐测序(WGBS)作为该领域具有重要意义的研究方法,将亚硫酸氢盐处理和下一代/第三代测序技术(主要是霰弹枪测序)相结合,在基因组水平上研究DNA甲基化。
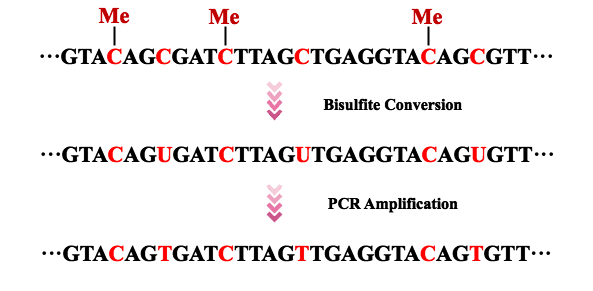
图1。在DNA测序之前进行亚硫酸氢盐转化和PCR扩增。
全基因组亚硫酸氢盐测序的优势
全基因组亚硫酸氢盐测序工作流程
简而言之,以下基本步骤 全基因组亚硫酸氢盐测序 (WGBS)包括DNA提取、亚硫酸氢盐转化、文库制备、测序和生物信息学分析。在这里,我们使用Illumina HiSeq作为示例来说明以下工作流程 WGBS.
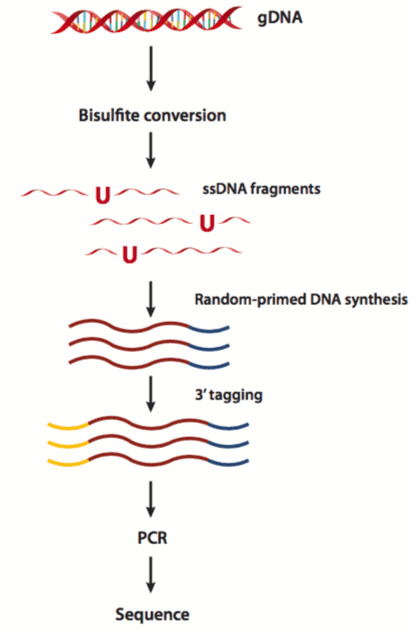
图2:全基因组亚硫酸氢盐测序的工作流程(Khanna 等. 2013).
首先,制备从人类、动物、植物或微生物收集的约1-5mg组织样本用于DNA。一般来说,用于全基因组亚硫酸氢盐测序的样本需要满足以下四个特征。
i.真核生物;
ii。低甲基化(如图3所示,研究表明,一旦一个区域中CpG位点的数量增加,WGBS的测序数据就开始减少);
iii.其参考基因组至少已组装到支架水平;
iv. Relatively complete genome annotations. And then, apply a suitable kit to extract high-purity and high-molecular-weight DNA. The extracted DNA should have a mass of no less than 5 μg, a concentration of no less than 50 ng/ul, and an OD260/280 of 1.8 to 2.0.

图3。传统的WGBS技术甲基化位点覆盖率低(Raine 等. 2016)
Bisulfite conversion is considered to be the “gold standard” for DNA methylation analysis, the principles have been shown in Figure 4. For this method, BS-induced DNA degradation may lead to depletion of genomic regions enriched for unmethylated cytosines. Therefore, it is important to assess the amount of DNA degradation under reaction conditions, and how this affects the desired amplicon should also be considered. Olova 等(2018)发现,在利用高变性或高亚硫酸氢盐摩尔浓度的亚硫酸氢酯转化方案中,DNA降解很强。市场上有几种试剂盒(表2)。
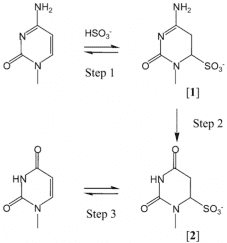
图4。亚硫酸氢盐介导胞嘧啶脱氨基(Hayatsu 等. 2004).
表2。亚硫酸氢盐转化协议和参数。
| 套件 | 变性 | 转化温度 | 孵育时间 |
| Zymo EZ DNA甲基化闪电试剂盒 | Heat-based; 99 °C Alkaline-based; 37 °C |
65 °C | 90分钟 |
| EpiTec亚硫酸氢盐试剂盒(Qiagen) | Heat-based; 99 °C | 55 °C | 10小时 |
| EZ DNA甲基化试剂盒(Zymo Research) | Alkaline-based; 37 °C | 50 °C | 12至16小时 |
以EpiGnome为例超在禅定 Methyl-Seq Kit (Epicentre) as an example (as shown in Figure 5), bisulfite-treated single-stranded DNA is random-primed using a polymerase capable of reading uracil nucleotides, to synthesize DNA containing a specific sequence tag. The 3’ end of the newly synthesized DNA strand is then selectively labeled with a second specific sequence, thus a two-marker DNA molecular with a known sequence tag at the 5’ and 3’ ends can be obtained. Illumina P7 and P5 adapters are subsequently added by PCR at the 5 and 3 ends prior to DNA sequencing.
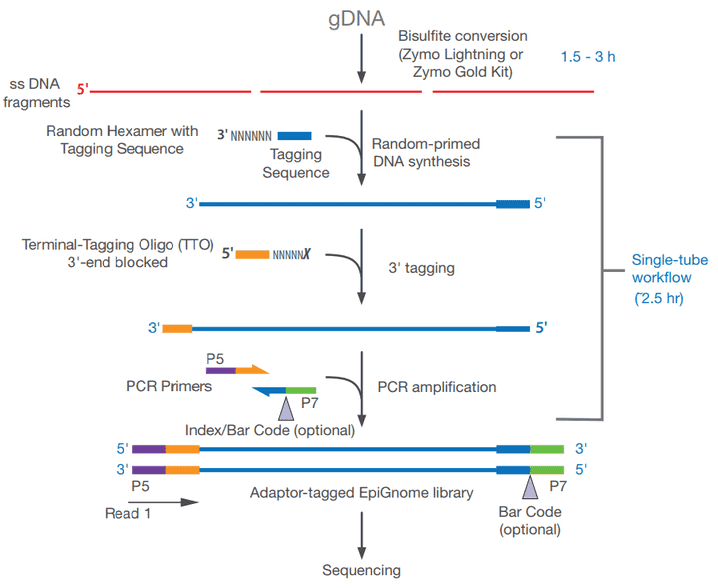
图5。EpiGnome的工作流程超在禅定 甲基序列试剂盒。
Hiseq测序技术是一种基于合成测序(SBS)的新型测序方法,广泛应用于WGBS。流动池上的桥放大是通过使用单分子阵列实现的。由于新的可逆阻断技术一次只能合成一个碱基并标记荧光团,因此使用相应的激光激发荧光团,并捕获激发光以读取碱基信息。WGBS中通常采用配对末端150bp策略对250-300bp插入亚硫酸氢盐处理的DNA文库进行测序。除了Illumina HiSeq之外, PacBio SMRT, 纳米孔罗氏454和其他Illumina平台也常用于此目的。
可以对测序结果进行一系列分析。表3列出了五种主要的信息分析类型。此外,还可以进行甲基化密度分析、差异甲基化区域(DMR)分析、DMR注释和富集分析(GO/KEGG)以及聚类分析。WGBS的常见生物信息资源包括BDPC、CpGcluster、CpGFinder、Epinexus、MethTools、mPod、QUMA和TCGA数据门户。
表3。WGBS数据分析的主要类型。
| 类型 | 详情 |
| 与参考基因组比对 | SOAP软件等工具用于将读取结果与参考基因组序列进行比较,只有对齐的读取结果才会用于分析甲基化信息。对齐读取允许C-C匹配和C-T不匹配。 |
| mC呼叫 | 确定mC在整个基因组中的位置。mC比率是通过考虑读取质量和多轨迹映射概率来计算的。丢弃对齐可靠性低的小概率对齐。 |
| 序列深度和覆盖率分析 | 反映基因覆盖率和测序深度之间关系的图像决定了是否可以在特定碱基位置以一定程度的置信度进行甲基化发现。 |
| 甲基化水平分析 | 每个甲基化C碱基的甲基化水平计算如下:100*读数/总读数。全基因组平均甲基化水平反映了基因组甲基化谱的总体特征。 |
| 甲基化的全球趋势 | CG、CHGG和CHH在甲基化C碱基中的分布比例在一定程度上反映了特定物种全基因组甲基化图谱的特征。 |
参考文献